研究紹介
医学物理グループでは、非剛体レジストレーション、CTベース肺機能画像、MRI-Linac、AIベース治療効果・副作用予測、 AIベース自動計画、AIベース患者QAの研究を主に行っております。特に、人工知能(AI)を含む高度な医用画像処理を用いた放射線治療支援システムの開発を精力的に行っており、非剛体レジストレーション、AIベース自動計画、AIベースバーチャル患者QA、AIベース治療効果予測などの技術は国内外の特許や製品化による社会実装を行っています。当研究室は、大きな研究成果を達成するために教員や大学院生の個々の研究が一本の線のように上手く繋がり、最終的に大きな研究成果が達成出来るよう全員が研究を行っており、大学院生の研究テーマもそれに則して決定しています。医学物理士としては、その研究成果を臨床にフィードバックさせ、最終的には患者の治療成績向上および副作用低減に繋げることが重要だと考え、そのことを医学物理部門の最大の目標としています。以下に主な研究プロジェクトの概要を示します。
目次
1. AIを用いた放射線治療プロセスのオートメーション化と個別医療に向けて
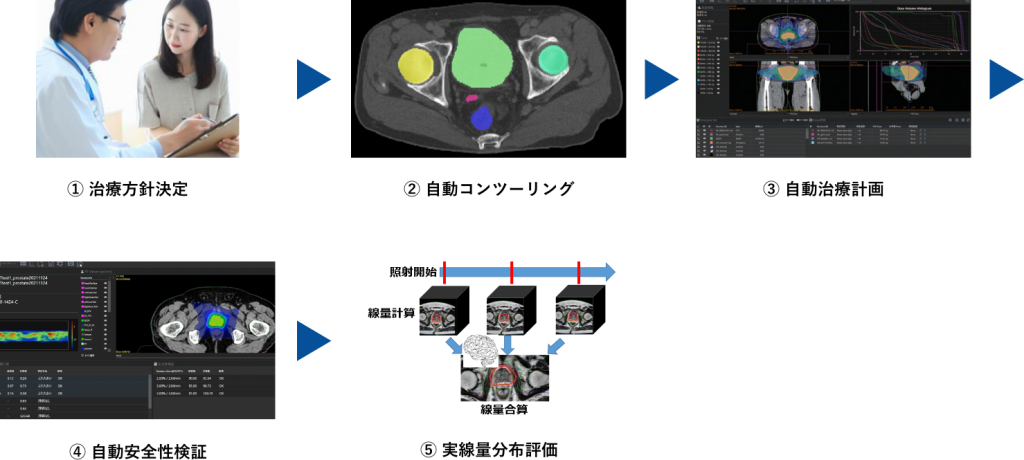
① 治療方針決定
② 自動コンツーリング
③ 自動治療計画
④ 自動安全性検証
⑤ 実線量分布評価
2. AI・DIRを用いた新たな画像イメージングの開発
① CTベース肺換気画像
② 放射線肺炎発生ハザードマップ
3. 非剛体レジストレーションを用いた自動輪郭抽出・合算線量分布評価システムの臨床評価・技術開発
4. MR-Linacによる即時適応放射線治療の臨床技術研究
1. AIを用いた放射線治療プロセスのオートメーション化と個別医療に向けて
① 治療方針決定
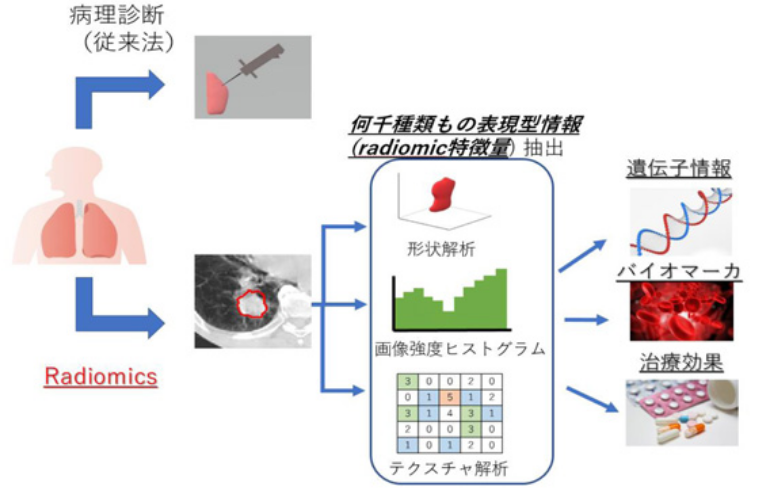
最新の画像処理技術とこれまでに治療した患者の大規模症例(ビックデータ)を用いて、高精度な放射線治療の予後予測(治療効果)、副作用発生、腫瘍の縮小を治療開始前に予測する研究・開発を行っています。この研究分野は、Radiomicsとも呼ばれており、医用画像のみからこれまでにはない高精度な予後予測を実現しようという研究です。我々の研究室のメンバーも多く執筆した国内発のradiomicsの書籍が発刊されています。これまでに、新たなradiomics特徴量を開発したり、ディープラーニングを用いて放射線治療による腫瘍縮小を予測する技術、さらに放射線肺臓炎を予測する技術を開発しています。
Key papers
・Tanaka S, Kadoya N, Sugai Y, Umeda M, Ishizawa M, Katsuta Y, Ito K, Takeda K, Jingu K, “A deep learning-based radiomics approach to predict head and neck tumor regression for adaptive radiotherapy”, Sci Rep. 2022 May 27;12(1):8899.
・Sugai Y, Kadoya N, Tanaka S, Tanabe S, Umeda M, Yamamoto T, Takeda K, Dobashi S, Ohashi H, Takeda K, Jingu K, “Impact of feature selection methods and subgroup factors on prognostic analysis with CT-based radiomics in non-small cell lung cancer patients”, Radiat Oncol. 2021 Apr 30;16(1):80.
・Kadoya N, Tanaka S, Kajikawa T, Tanabe S, Abe K, Nakajima Y, Yamamoto T, Takahashi N, Takeda K, Dobashi S, Takeda K, Nakane K, Jingu K, “Homology-based Radiomic Features for Prediction of the Prognosis of Lung Cancer Based on CT-based Radiomics”, Med Phys. 2020 Feb 25
・Tanaka S, Kadoya N, Kajikawa T, Matsuda S, Dobashi S, Takeda K, Jingu K. Investigation of thoracic four-dimensional CT-based dimension reduction technique for extracting the robust radiomic features. Phys Med. 2019 Feb;58:141-148.
プレスリリース
コップ=輪っか?:ホモロジー解析技術による新規画像… | プレスリリース・研究成果 | 東北大学 -TOHOKU UNIVERSITY-
放射線治療の個別化医療実現へ 深層学習で頭頸部癌の… | プレスリリース・研究成果 | 東北大学 -TOHOKU UNIVERSITY-
研究助成
・公益財団法人テルモ生命科学振興財団 研究開発助成金 (2023年4月~2024年3月、研究代表者 角谷倫之、200万円)
・科学研究費補助金 基盤C 「頭頸部がん個別化医療に向けた臨床情報とラジオミクス特徴量誘導適応放射線治療の研究」 (2021年4月~2024年3月、研究代表者 武田賢、研究分担者:角谷倫之)(保健学科放射線治療学分野との共同研究)
・科学研究費補助金 基盤C 「Radiomics技術を用いてCT画像のみから肺機能画像を作成する手法の開発」 (2019年4月~2023年3月、研究代表者 角谷倫之、429万円)
・科学研究費補助金 研究活動スタート支援 「患者個別化医療に向けた治療前の医療画像のみから腫瘍の縮小を予測する手法の開発」(2020年9月~2023年3月、研究代表者 田中祥平、273万円)
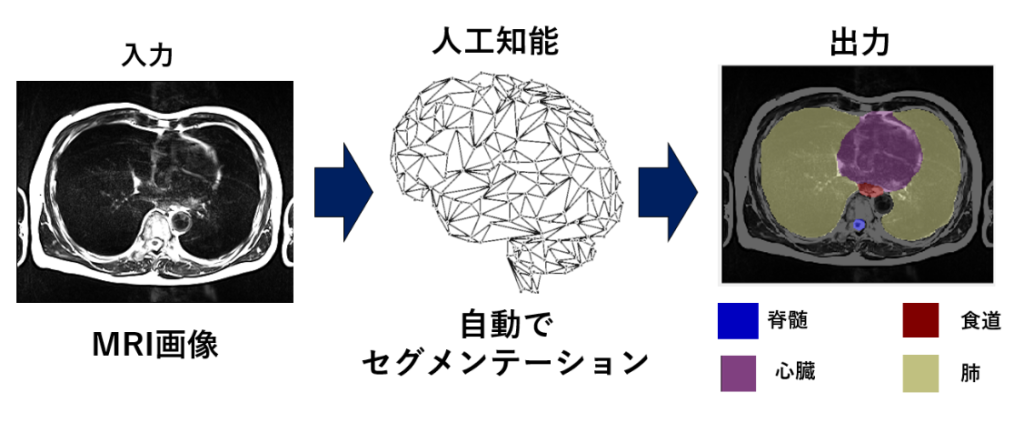
② 自動コンツーリング
最新の画像処理技術とこれまでに治療した患者の大規模症例(ビックデータ)を用いて、高精度な自動コンツーリング技術の研究・開発を行っています。このコンツーリング(輪郭作成)は、放射線治療には必ず必要な作業であり、CTやMR画像の各スライスに腫瘍やリスク臓器の輪郭を描いていく作業であり、頭頚部腫瘍のようにリスク臓器が多い部位などでは、一症例あたり3時間ほどコンツールに時間がかかることも珍しくありません。それをAIを含む高度画像処理を使って自動でコンツーリングできる技術を開発し、業務効率および医療スタッフ間の輪郭作成のばらつきを低減させることを目指しています。
研究助成
・ NEDO Entrepreneurs Program (NEP) タイプ B (2022年8月~2023年3月、アイラト株式会社、2500万円、分担研究)
・公益財団法人がん研究振興財団がん研究助成金 (2018年1月~2018年12月、研究代表者 高山佳樹、50万円)
書籍
・Iori Sumida et al. “Artificial Intelligence in Radiation Therapy (Ipem-iop Series in Physics and Engineering in Medicine and Biology”, Inst of Physics Pub Inc (2023/2/28) (Co-author, Noriyuki Kadoya)
Artificial Intelligence in Radiation Therapy
③ 自動治療計画
AI (深層学習)を用いて最適な治療計画を自動で生成する技術を開発しています。CTや輪郭情報を入力するだけで、学習された治療計画データを基に最適な治療計画を生成する技術です(下図)。

最適な線量分布を予測する技術については、頭頚部、胸部、前立腺、子宮頸癌においてAIモデルを開発し、産学連携で社会実装されています。近年では、深層強化学習による次世代型のAIモデル開発にも着手しています。
Key papers
・Kajikawa T, Kadoya N, Ito K, Takayama Y, Chiba T, Tomori S, Nemoto H, Dobashi S, Takeda K, Jingu K. A convolutional neural network approach for IMRT dose distribution prediction in prostate cancer patients. J Radiat Res. 2019 Oct 23;60(5):685-693. doi: 10.1093/jrr/rrz051. PMID: 31322704; PMCID: PMC6805973.
・Kajikawa T, Kadoya N, Ito K, Takayama Y, Chiba T, Tomori S, Takeda K, Jingu K. Automated prediction of dosimetric eligibility of patients with prostate cancer undergoing intensity-modulated radiation therapy using a convolutional neural network. Radiol Phys Technol. 2018 Sep;11(3):320-327.
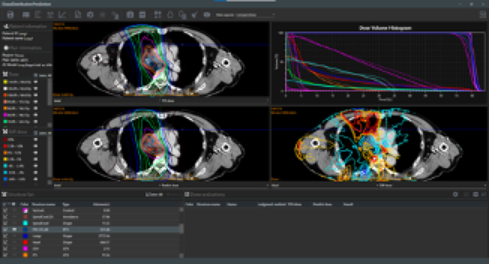
社会実装されたAIによる線量分布予測システム, AIVOT-QA (アイラト社)
プロダクト – アイラト株式会社(AiRato) – 放射線治療AIで医療DXを支援
メディア
・テレビ東京 World business satellite (WBS) 「AIで進化するがん治療 最新テック×医療の未来
https://www.tv-tokyo.co.jp/mv/wbs/feature/post_273425/ (2023.5.4)
研究助成
・公益財団法人テルモ生命科学振興財団 研究開発助成金 (2023年4月~2024年3月、研究代表者 角谷倫之、200万円)
・科学研究費補助金 基盤C 「深層強化学習による真の“人工知能型”自動放射線照射計画法の開発」(2023年4月~2026年3月、研究代表者 角谷倫之、500万円)
・NEDO Entrepreneurs Program (NEP) タイプ B (2022年8月~2023年3月、アイラト株式会社、2500万円、分担研究)
④ 自動安全性検証(バーチャル患者個別QA)
AI (深層学習)を用いて作成された治療計画のデータから自動で計画通りに照射できるかどうか(安全に照射できるかどうか)を判定する技術を開発しています。作成された治療計画データを入力するだけで、実測検証によって安全に照射できるかが既にわかる治療計画データを基に学習されたAIモデルが安全性検証結果(ガンマパス率)を予測する技術です(下図)。
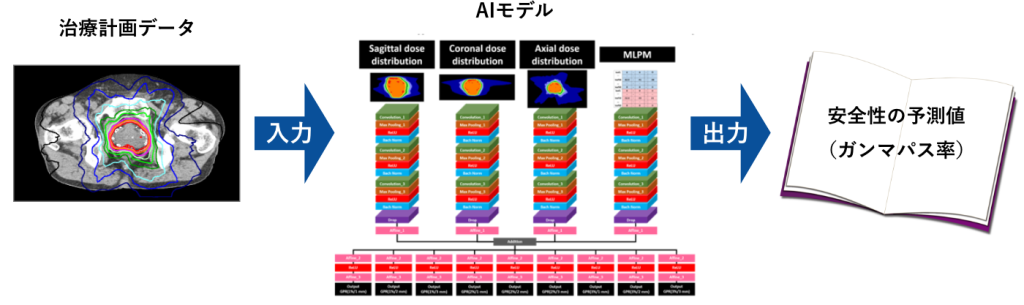
頭頚部、前立腺において既にAIモデルを開発し、産学連携で社会実装されています。近年では、治療計画データから精度よく安全検証結果を予測する新たな最適な入力値の開発を行っています。
Key papers
・Tozuka R, Kadoya N, Tomori S, Kimura Y, Kajikawa T, Sugai Y, Xiao Y, Jingu K, “Improvement of deep learning prediction model in patient-specific QA for VMAT with MLC leaf position map and patient’s dose distribution”, J Appl Clin Med Phys. 2023 Jun 1;e14055
・Tomori S, Kadoya N, Kajikawa T, Kimura Y, Narazaki K, Ochi T, Jingu K. Systematic method for a deep learning-based prediction model for gamma evaluation in patient-specific quality assurance of volumetric modulated arc therapy. Med Phys. 2021 Mar;48(3):1003-1018. doi: 10.1002/mp.14682. Epub 2021 Jan 28. PMID: 33368406.
・Kimura Y, Kadoya N, Tomori S, Oku Y, Jingu K. Error detection using a convolutional neural network with dose difference maps in patient-specific quality assurance for volumetric modulated arc therapy. Phys Med. 2020 May;73:57-64.
・Tomori S, Kadoya N, Takayama Y, Kajikawa T, Shima K, Narazaki K, Jingu K. A deep learning-based prediction model for gamma evaluation in patient-specific quality assurance. Med Phys. 2018 Jul 31.
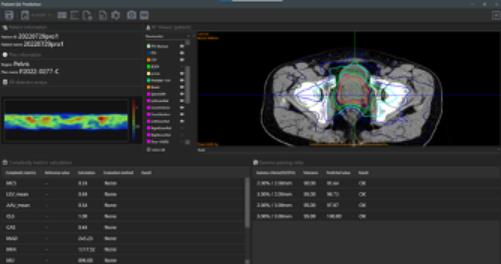
社会実装されたAIによる線量分布予測システム, AIVOT-QA (アイラト社)
プロダクト – アイラト株式会社(AiRato) – 放射線治療AIで医療DXを支援
研究助成
・NEDO Entrepreneurs Program (NEP) タイプ B (2022年8月~2023年3月、アイラト株式会社、2500万円、分担研究)
⑤ 実線量分布評価
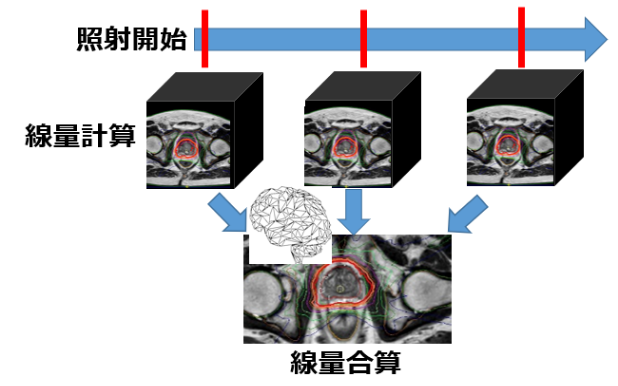
AI (深層学習)やログファイルを用いて、照射中の体内臓器の変化や機械的動作を反映した、リアルな患者への実線量分布評価法を研究・開発しています(下図)。これによって、MR-Linacなどで実施できる即時適応放射線治療(On-line ART)でのリアルな患者への照射線量を評価することができます。
Key papers
・Katsuta Y, Kadoya N, Fujita Y, Shimizu E, Majima K, Matsushita H, Takeda K, Jingu K. Log file-based patient dose calculations of double-arc VMAT for head-and-neck radiotherapy. Phys Med. 2018 Apr;48:6-10. doi: 10.1016/j.ejmp.2018.03.006. Epub 2018 Mar 20. PMID: 29728230.
・Kadoya N, Kon Y, Takayama Y, Matsumoto T, Hayashi N, Katsuta Y, Ito K, Chiba T, Dobashi S, Takeda K, Jingu K. Quantifying the performance of two different types of commercial software programs for 3D patient dose reconstruction for prostate cancer patients: Machine log files vs. machine log files with EPID images. Phys Med. 2018 Jan;45:170-176.
・Katsuta Y, Kadoya N, Fujita Y, Shimizu E, Matsunaga K, Matsushita H, Majima K, Jingu K. Clinical impact of dosimetric changes for volumetric modulated arc therapy in log file-based patient dose calculations. Phys Med. 2017 Oct;42:1-6.
・Katsuta Y, Kadoya N, Fujita Y, Shimizu E, Matsunaga K, Matsushita H, Majima K, Jingu K. Quantification of residual dose estimation error on log file-based patient dose calculation. Phys Med. 2016 May;32(5):701-5.
研究助成
・科学研究費補助金 基盤C 「深層学習技術による照射中の動きを考慮した本当の線量分布の作成」(2023年4月~2028年3月、研究代表者 田中祥平、481万円)
2. AI・DIRを用いた新たな画像イメージングの開発
① CTベース肺換気画像
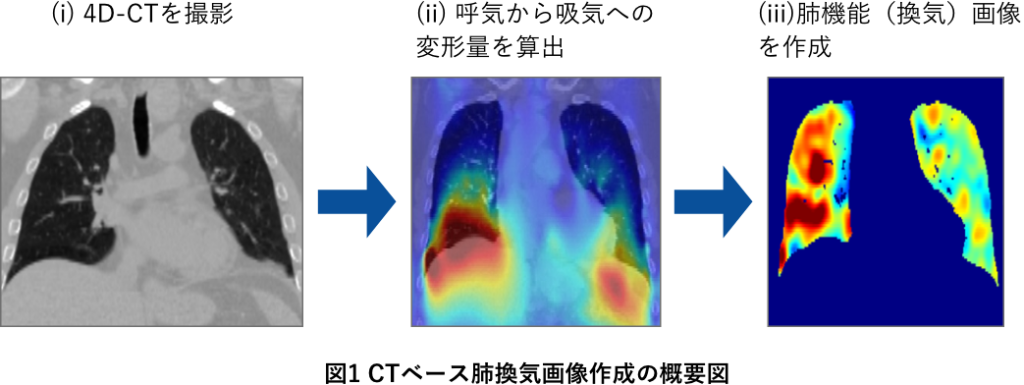
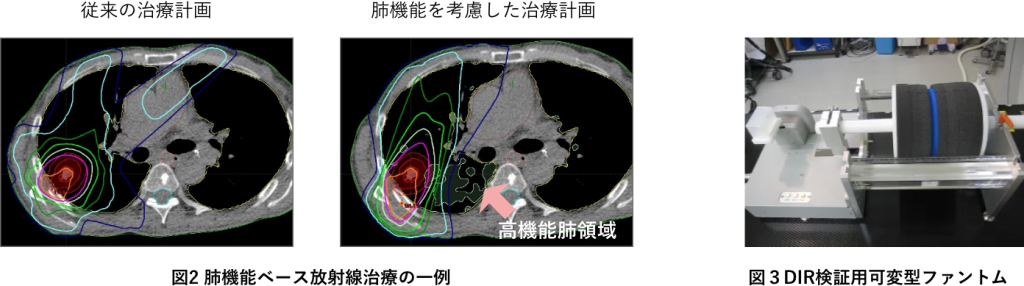
肺機能画像を放射線治療に応用し、肺機能が高いと判断された領域を避けて放射線を照射することで、肺障害を低減しつつ腫瘍への効果的な放射線照射が可能になると報告されています。従来、肺機能画像を取得する方法には、我々が提案する四次元断層撮影(4D-CT)画像を用いた方法以外に、核医学の画像、酵素ガス造影MRI、キセノンガスを用いたCT画像があります。しかし、これらの方法は、時間がかかる、低分解能、コストが高いなどの理由により普及していないのが現状です。そこで今回我々が提案する方法は、4D-CTとdeformable image registration (DIR)の画像処理技術を用いて肺の体積変化から肺機能画像を作成するという今までにはない新たな手法を用いた肺機能画像を取得する方法であり、この方法では、上記した肺機能画像を取得するための問題点を解決できると考えられます(下図)。まず、多くの病院に導入されている通常のCT装置を使用した4D-CT画像のみを利用することで、追加検査の必要がなく、”free”な情報から早く、高分解能な機能画像が作成できます。この利点より、現在行われている肺機能画像の取得方法よりも広く受け入れられる可能性が高く、多くの施設で肺機能を考慮した放射線治療を実現できると期待されています。我々の研究グループでは、この4D-CTとDIRから作成される肺機能画像を用いた放射線治療の有効性の検討、DIRの精度評価、肺機能の精度評価を行い臨床利用に向けた開発・解析を行っています。この高精度な肺機能画像を用いることで、未だ解明されていない肺への放射線の影響を解明できる可能性があります。近年では、広島大学・高知大学との共同研究においてこの肺機能画像を用いた臨床試験を開始しております。また、臨床利用を想定し、DIR検証用可変型肺ファントムの開発も行っています。
・Ieko Y, Kadoya N, Sugai Y, Mouri S, Umeda M, Tanaka S, Kanai T, Ichiji K, Yamamoto T, Ariga H, Jingu K. Assessment of a computed tomography-based radiomics approach for assessing lung function in lung cancer patients. Phys Med. 2022 Sep;101:28-35.
・ Kajikawa T, Kadoya N, Maehara Y, Miura H, Katsuta Y, Nagasawa S, Suzuki G, Yamazaki H, Tamaki N, Yamada K. A deep learning method for translating 3DCT to SPECT ventilation imaging: First comparison with 81m Kr-gas SPECT ventilation imaging. Med Phys. 2022 Jul;49(7):4353-4364
・Kadoya N, Nemoto H, Kajikawa T, Nakajima Y, Kanai T, Ieko Y, Ikeda R, Sato K, Dobashi S, Takeda K, Jingu K. Evaluation of four-dimensional cone beam computed tomography ventilation images acquired with two different linear accelerators at various gantry speeds using a deformable lung phantom. Phys Med. 2020 Sep;77:75-83.
・Kipritidis J, Tahir BA, Cazoulat G, Hofman MS, Siva S, Callahan J, Hardcastle N, Yamamoto T, Christensen GE, Reinhardt JM, Kadoya N, Patton TJ, Gerard SE, Duarte I, Archibald-Heeren B, Byrne M, Sims R, Ramsay S, Booth JT, Eslick E, Hegi-Johnson F, Woodruff HC, Ireland RH, Wild JM, Cai J, Bayouth JE, Brock K, Keall PJ. The VAMPIRE challenge: A multi-institutional validation study of CT ventilation imaging. Med Phys. 2019 Mar;46(3):1198-1217.
・Faught AM, Miyasaka Y, Kadoya N, Castillo R, Castillo E, Vinogradskiy Y, Yamamoto T. Evaluating the Toxicity Reduction With Computed Tomographic Ventilation Functional Avoidance Radiation Therapy. Int J Radiat Oncol Biol Phys. 2017 Oct 1;99(2):325-333.
・Kanai T, Kadoya N, Ito K, Kishi K, Dobashi S, Yamamoto T, Umezawa R, Matsushita H, Takeda K, Jingu K. Evaluation of four-dimensional computed tomography (4D-CT)-based pulmonary ventilation: The high correlation between 4D-CT ventilation and (81m)Kr-planar images was found. Radiother Oncol. 2016 Jun;119(3):444-8.
研究助成
・科学研究費補助金 基盤B 「局所進行非小細胞肺癌に対する肺機能画像を用いたオーダーメイド放射線治療法の開発 」(2020年4月~2024年3月、研究代表者 木村智樹、研究分担者:角谷倫之) (広島大学・高知大学との共同研究)
・科学研究費補助金 基盤C 「肺癌に対する機能的画像を用いたオーダーメイド放射線治療法の臨床応用」(2017年4月~2020年3月、研究代表者 木村智樹、研究分担者:角谷倫之) (広島大学木村先生との共同研究)
・東北大学病院 若手研究者による臨床応用研究推進プログラム (2015年4月~2017年3月、研究代表者 角谷倫之、200万円)
・日本医学放射線学会 バイエル研究助成 (2014年4月~2015年3月、研究代表者 角谷倫之, 100万円)
・科学研究費補助金 若手B 「四次元断層撮影画像による肺機能画像の開発と放射線治療への応用」(2012年4月~2014年3月、研究代表者 角谷倫之、390万円)
② 放射線肺炎発生ハザードマップ
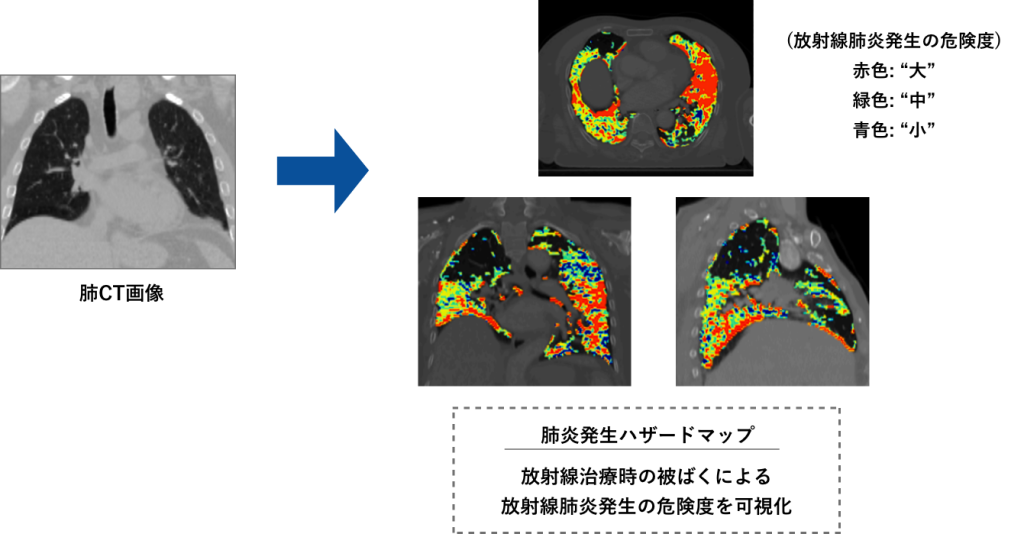
CT画像とAIを活用して、被ばくによる重篤な肺炎の恐れを予測する“ハザードマップ”の開発を行っています(下図)。この技術をVMAT(回転強度変調放射線治療)に応用し、ハザードマップが危険と表示した肺組織の被ばくを低減することが可能となります。この放射線治療は肺がん放射線治療の低侵襲化および治療効果向上が期待されます。
・Katsuta Y, Kadoya N, Kajikawa T, Mouri S, Kimura T, Takeda K, Yamamoto T, Imano N, Tanaka S, Ito K, Kanai T, Nakajima Y, Jingu K. Radiation pneumonitis prediction model with integrating multiple dose-function features on 4DCT ventilation images. Phys Med. 2023 Jan;105:102505.
・Katsuta Y, Kadoya N, Sugai Y, Katagiri Y, Yamamoto T, Takeda K, Tanaka S, Jingu K. Feasibility of Differential Dose-Volume Histogram Features in Multivariate Prediction Model for Radiation Pneumonitis Occurrence. Diagnostics (Basel). 2022 May 31;12(6):1354.
・Katsuta Y, Kadoya N, Mouri S, Tanaka S, Kanai T, Takeda K, Yamamoto T, Ito K, Kajikawa T, Nakajima Y, Jingu K. Prediction of radiation pneumonitis with machine learning using 4D-CT based dose-function features. J Radiat Res. 2022 Jan;63:71-79.
研究助成
・科学研究費補助金 若手B 「肺の機能と形態の線量評価を融合した放射線肺臓炎予測モデルの構築」(2020年4月~2024年3月、研究代表者 勝田義之、299万円)
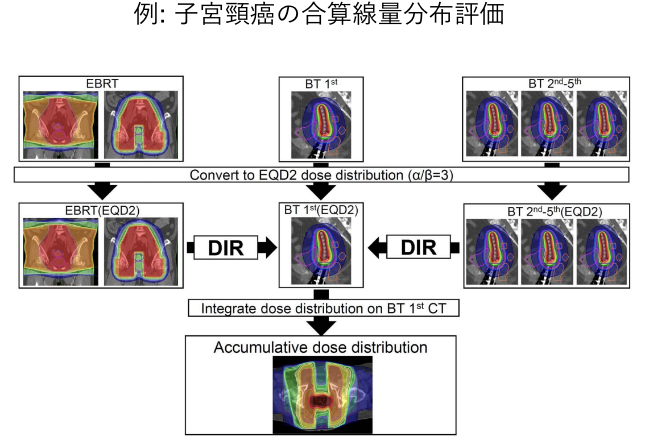
3. 非剛体レジストレーションを用いた自動輪郭抽出・合算線量分布評価システムの臨床評価・技術開発
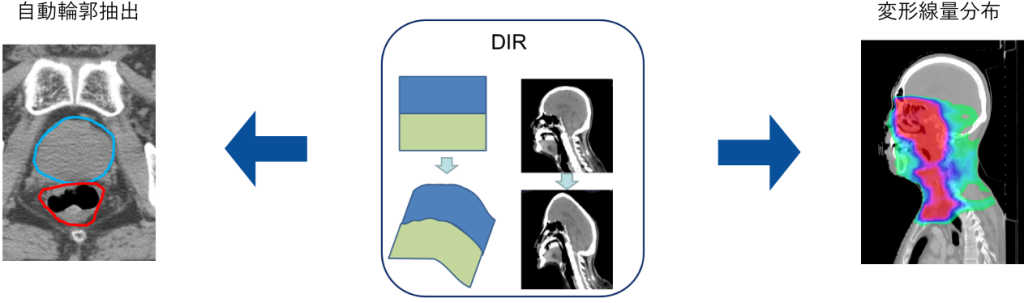
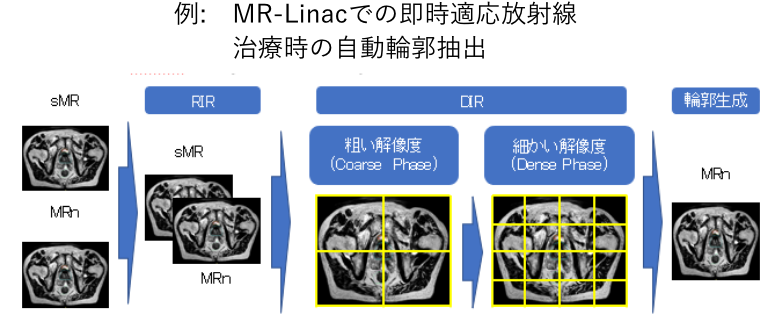
非剛体レジストレーション (DIR)を使った自動輪郭抽出や合算線量分布評価の臨床評価・技術開発を行っています。CT-CT間、CT-MR間、MR-MR間のDIRを活用することでCTやMR画像上に輪郭を自動生成できたり、それぞれの画像で計算された線量分布を高精度に合算することができます。この技術を用いることで、より迅速なコンツーリングが可能となり、またより正確な患者への線量評価が可能となります。RALSやMR-Linacで積極的に臨床利用および研究を行っています(下図)。我々の研究室のメンバーも多く執筆した国内発の放射線治療領域のDIRの書籍も発刊されています。

社会実装されたDIR検証用物理ファントム,
忍者ファントム(東洋メディック社)
・Miyasaka Y, Kadoya N, Umezawa R, Takayama Y, Ito K, Yamamoto T, Tanaka S, Dobashi S, Takeda K, Nemoto K, Iwai T, Jingu K. Comparison of predictive performance for toxicity by accumulative dose of DVH parameter addition and DIR addition for cervical cancer patients. J Radiat Res. 2021 Jan 1;62(1):155-162.
・Sugawara Y, Kadoya N, Kotabe K, Nakajima Y, Ikeda R, Tanabe S, Ohashi H, Jingu K. Development of a dynamic deformable thorax phantom for the quality management of deformable image registration. Phys Med. 2020 Sep;77:100-107.
・Kadoya N, Miyasaka Y, Nakajima Y, Kuroda Y, Ito K, Chiba M, Sato K, Dobashi S, Yamamoto T, Takahashi N, Kubozono M, Takeda K, Jingu K. Evaluation of deformable image registration between external beam radiotherapy and HDR brachytherapy for cervical cancer with a 3D-printed deformable pelvis phantom. Med Phys. 2017 Apr;44(4):1445-1455.
・Kadoya N, Nakajima Y, Saito M, Miyabe Y, Kurooka M, Kito S, Fujita Y, Sasaki M, Arai K, Tani K, Yagi M, Wakita A, Tohyama N, Jingu K. Multi-institutional Validation Study of Commercially Available Deformable Image Registration Software for Thoracic Images. Int J Radiat Oncol Biol Phys. 2016 Oct 1;96(2):422-431.
・Kadoya N, Fujita Y, Katsuta Y, Dobashi S, Takeda K, Kishi K, Kubozono M, Umezawa R, Sugawara T, Matsushita H, Jingu K. Evaluation of various deformable image registration algorithms for thoracic images. J Radiat Res. 2014 Jan 1;55(1):175-82.
研究助成
・科学研究費補助金 国際共同研究強化B 「国際医学物理ネットワークを軸とした放射線治療における先端技術の創出と普及」(2018年10月~2023年3月、研究代表者 中村光宏、研究分担者:角谷倫之) (京都大学医学系研究科 中村研究室との共同研究)
・科学研究費補助金 若手B 「子宮頸がんに対する外部照射と腔内照射の高精度な積算線量評価システムの開発」(2015年4月~2019年3月、研究代表者 角谷倫之、403万円)
(大阪大学基礎工の大城研究室と共同研究)
・マイクロセレクトロンHDR研究会研究助成 (2014年1月~2015年12月、研究代表者 角谷倫之、100万円)
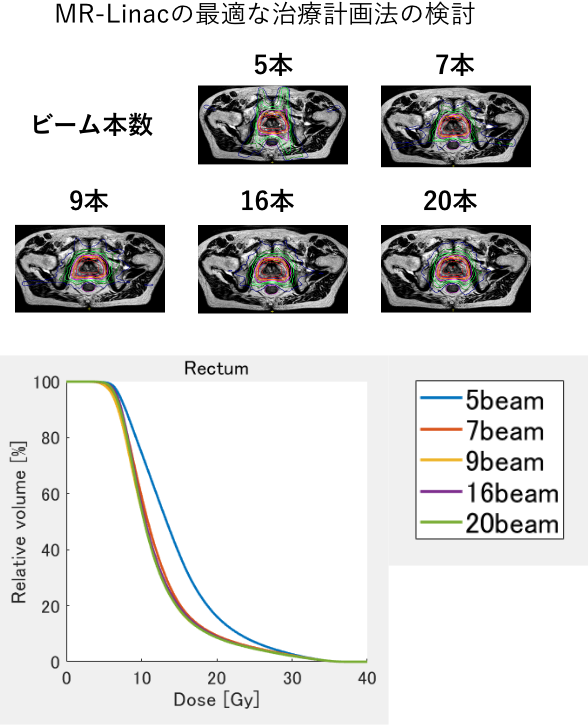
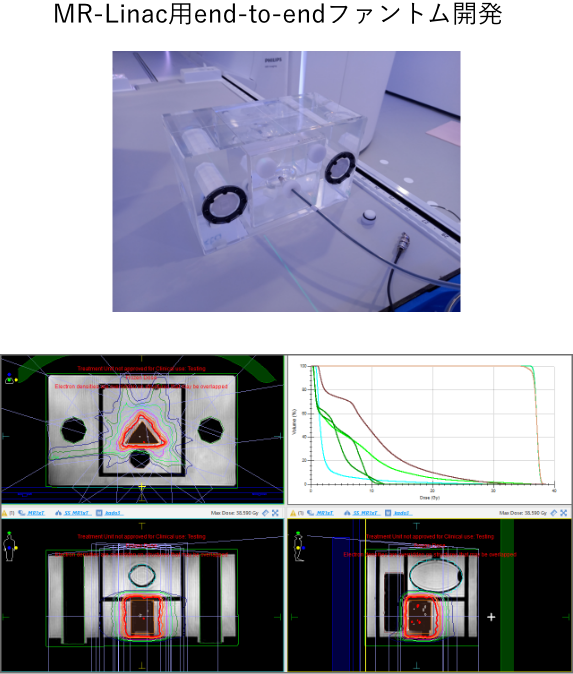
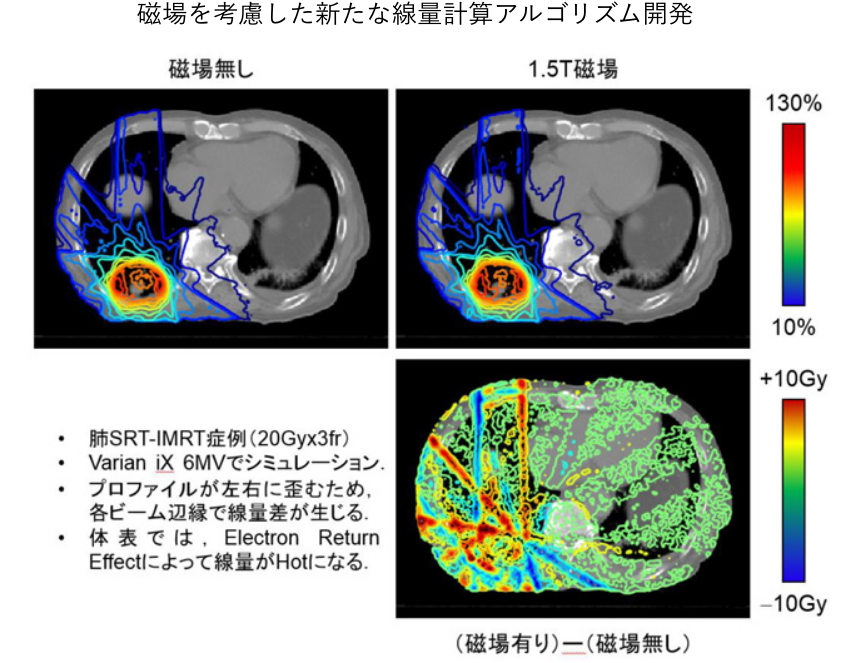
4. MR-Linacによる即時適応放射線治療の臨床技術研究
MR-Linacを用いた最適な治療計画法の検討や、MR画像を使った最適な線量計算手法の開発、即時適応放射線治療のend-to-endファントムの開発などを行っています(下図)。
・Okamoto H, Igaki H, Chiba T, Shibuya K, Sakasai T, Jingu K, Inaba K, Kuroda K, Aoki S, Tatsumi D, Nakamura M, Kadoya N, Furuyama Y, Kumazaki Y, Tohyama N, Tsuneda M, Nishioka S, Itami J, Onishi H, Shigematsu N, Uno T. Practical guidelines of online MR-guided adaptive radiotherapy. J Radiat Res. 2022 Sep 21;63(5):730-740.
・Ito K, Kadoya N, Katsuta Y, Tanaka S, Dobashi S, Takeda K, Jingu K. Evaluation of the electron transport algorithm in magnetic field in EGS5 Monte Carlo code. Phys Med. 2022 Jan;93:46-51.
・Kajikawa T, Kadoya N, Tanaka S, Nemoto H, Takahashi N, Chiba T, Ito K, Katsuta Y, Dobashi S, Takeda K, Yamada K, Jingu K. Dose distribution correction for the influence of magnetic field using a deep convolutional neural network for online MR-guided adaptive radiotherapy. Phys Med. 2020 Dec;80:186-192.
研究助成
・科学研究費補助金 若手研究 「MRI-Linac用NonlinearCCC線量計算アルゴリズムの開発」(2018年4月~2020年3月、研究代表者 伊藤謙吾, 351万円)
・科学研究費補助金 若手(B) 「定量的磁化率マッピングを用いた高精度線量計算システムの開発」(2015年4月~2017年3月、研究代表者 伊藤謙吾、403万円